






Одним из наиболее широко известных флуороген-активирующих белков является белок FAST, разработанный во Франции. FAST имеет сравнительно малый размер и способен взаимодействовать с широким спектром флуорогенов. Тем не менее, его пространственная структура до последнего времени оставалась неизученной. Поэтому на первом этапе работы стояла задача получить трехмерную структуру FAST в комплексе с одним из флуорогенов - N871b. Эту задачу удалось решить с использованием спектроскопии ядерного магнитного резонанса, определив как пространственную структуру комплекса FAST/N871b, так и структуру FAST в "свободном" состоянии. Оказалось, что флуороген существенным образом стабилизирует FAST. Без него часть белка становится подвижной и теряет свою спиральную структуру. Что интересно, эта часть FAST напрямую не участвует во взаимодействии с флуорогеном. Это навело ученых на мысль, что белок FAST можно укоротить на 30% без потери его функциональности, так появилась концепция белка nanoFAST.

Пространственные структуры FAST и nanoFAST, в свободном состоянии и в комплексе с флуорогенами N871B и HBR-DOM2. Источник: пресс-служба ИБХ РАН
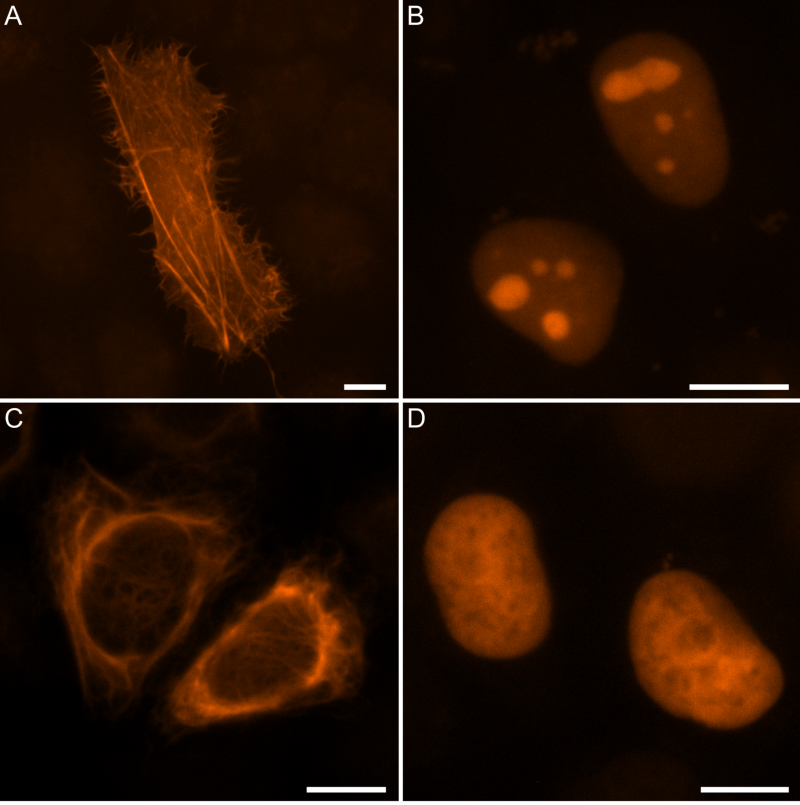
Первые эксперименты оказались не обнадеживающими - nanoFAST не работал в паре со всеми известными флуорогенами FAST. Чтобы решить эту проблему, сотрудники института синтезировали библиотеку потенциальных флуорогенов, состоящую из 40 различных соединений схожей природы. Одно из соединений, HBR-DOM2, оказалось способно взаимодействовать с nanoFAST с образованием флуоресцирующего комплекса, яркость флуоресценции не уступала комплексам "материнского" белка FAST с известными флуорогенами. Авторам удалось продемонстрировать, что пару nanoFAST/HBR-DOM2 можно использовать для исследования живых объектов - были проведены эксперименты по флуоресцентному окрашиванию живых человеческих клеток HeLa c визуализацией нескольких клеточных белков (Рис. 2).
Таким образом, была создана самая маленькая генетически кодируемая флуоресцентная метка, nanoFAST.
